為何蒸汽溫度低于飽和溫度?
在許多工廠之中,總是遇著這般的問題:明明用的是飽和蒸汽,可測得的溫度總是比相應壓力所對應的飽和溫度低了不少。這是為什么呢?是不是儀表測量不準呢?可能儀表確實有故障,但還有另外一種可能,即是儀表所顯示的值并沒有錯,而是蒸汽里面混有不少空氣等不凝性氣體。
怎么,混入空氣之后蒸汽溫度也會降低?
我們可以用另一種思路來想這個問題,而這便牽涉到道爾頓分壓定律了。
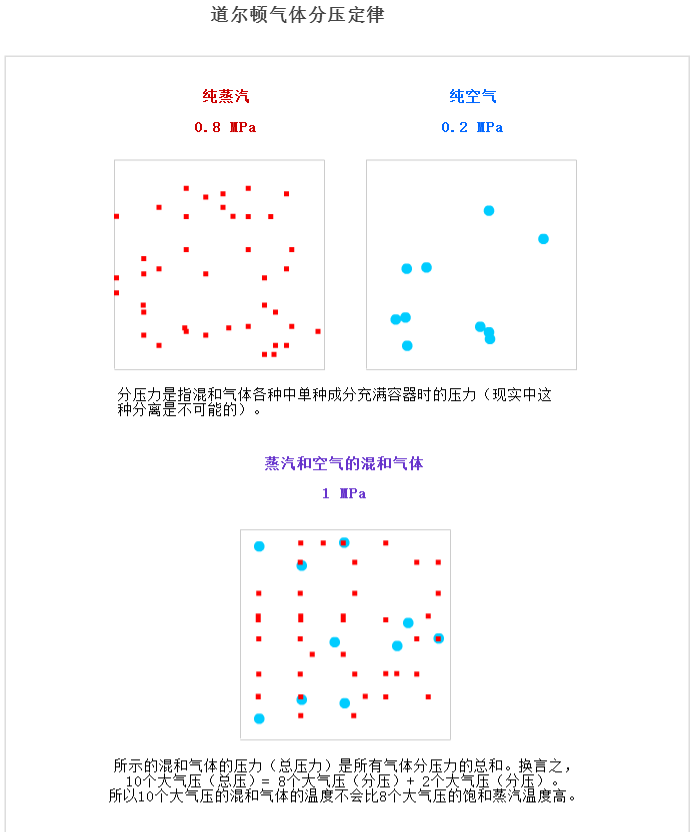
道爾頓分壓定律怎么說的呢?理想混合氣體的總壓力等于各組元氣體分壓力之總和。照著道爾頓分壓定律的說法,我們可以知道,如果飽和蒸汽之中混入不少空氣或其它不可凝氣體,那么它們就組成了一種混合氣體。壓力測點所能顯示的是混合氣體的壓力,混合氣體的壓力又是高于飽和蒸汽的分壓。
于是,我們不能簡單地使用壓力測點顯示的壓力值來衡量蒸汽溫度,如果飽和蒸汽分壓比混合氣體壓力低不少,那自然而然地蒸汽溫度得比測點壓力對應的蒸汽飽和溫度低不少。
這個事例提醒我們,如果不能確保蒸汽品質,不可輕易地利用壓力測點顯示的壓力值來估計蒸汽溫度。更重要的是,注意提高蒸汽品質,在管道高處、管道末端科學安裝排空氣閥。